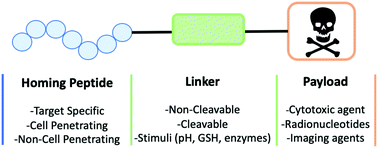
Malgré les progrès continus dans le traitement des conjugués anticorps-médicament (ADC), plusieurs défis demeurent. Par exemple, la structure complexe des ADC entraîne des coûts de production élevés et une longue demi-vie, ce qui augmente la toxicité systémique en raison d’une exposition prolongée dans le plasma. Par conséquent, les conjugués peptide-médicament (PDC) sont apparus comme une alternative prometteuse. Les PDC se composent de trois composants : un peptide hôte, un lieur et un médicament à charge utile. Utilisant la grande affinité des peptides locaux pour les récepteurs de la surface tumorale, les PDC délivrent la charge utile du médicament directement à la cible.

Formes de charges utiles PDC
Les PDC peuvent transporter diverses formes de charges utiles. Il peut s'agir de médicaments de chimiothérapie conventionnels comme le paclitaxel ou la gemcitabine. Les isotopes radioactifs sont également utilisés pour le diagnostic précis des maladies et la radiothérapie ciblée. Les isotopes de diagnostic comprennent le fluor-18 (18F), le cuivre-64 (64Cu), le gallium-68 (68Ga) et l'iode-123 (123I). Ces isotopes, conjugués à des peptides ciblants, se lient aux récepteurs des cellules tumorales, permettant une localisation précise des tissus malins grâce à la détection des positrons libérés par les isotopes. Lorsque les peptides ciblés sont liés à des isotopes radioactifs tels que l'Indium-111 (111In), l'Yttrium-90 (90Y) et le Lutétium-177 (177Lu), les PDC fonctionnent comme des agents de radiothérapie ciblés. Les autres charges utiles pour les PDC comprennent les protéines, les anticorps, les peptides et les acides nucléiques.

Avantages des PDC
Les PDC présentent des similitudes avec les ADC mais surmontent certaines de leurs limites. Comparés aux ADC, les PDC ont un poids moléculaire plus petit, une meilleure pénétration tissulaire et une immunogénicité faible ou nulle. De plus, les PDC sont plus faciles à synthétiser, purifier et identifier, ce qui entraîne des coûts de production inférieurs. Grâce aux progrès de la technologie de cyclisation, de la technologie d’affichage sur phage et de la technologie d’affichage d’ARNm pour cibler la sélection des peptides, le développement de médicaments PDC s’est accéléré. Les PDC sont sur le point de devenir la prochaine génération de médicaments ciblés, après les médicaments ciblés à petites molécules, les anticorps et les ADC.
Caractéristiques pharmacocinétiques des PDC
AbsorptionLes PDC ont un poids moléculaire relativement élevé et une faible perméabilité par rapport aux petites molécules traditionnelles. En raison de l’instabilité de leurs peptides dans le tractus gastro-intestinal, les PDC actuellement sur le marché et au stade clinique sont administrés par voie intraveineuse, contournant ainsi le processus d’absorption. Ils peuvent également être administrés par voie sous-cutanée ou intramusculaire, en pénétrant dans le système sanguin ou lymphatique. Un inconvénient majeur des PDC en tant que médicaments est leur instabilité et leur courte demi-vie in vivo, car les peptides sont rapidement dégradés par les protéases et facilement éliminés par les reins. Ceci est particulièrement problématique dans le traitement des tumeurs solides, où une circulation prolongée est nécessaire pour une pénétration adéquate du tissu tumoral. La modification des peptides pour améliorer la stabilité et prolonger la demi-vie est une stratégie cruciale.
DistributionLes peptides PDC sont classés en deux types : les peptides ciblant les cellules (CTP) et les peptides pénétrant les cellules (CPP). En raison de la faible spécificité des CPP pour les cellules, ils ne sont généralement pas utilisés comme peptides de référence dans les PDC. Les PDC ciblent les tumeurs de deux manières : 1) les PDC se lient aux récepteurs surexprimés à la surface des cellules tumorales, pénètrent dans les cellules par endocytose et libèrent des toxines dans les lysosomes ; 2) Les PDC libèrent des toxines dans l’environnement tumoral, qui pénètrent ensuite dans les cellules tumorales et les tuent.
MétabolismeLes PDC sont métabolisés in vivo via trois voies principales :
- Disposition des médicaments à médiation cible (TMDD) : Le TMDD est une voie d'élimination spécifique. Les PDC se lient aux récepteurs des cellules cibles, sont internalisés et dégradés en acides aminés et peptides dans les lysosomes. Cependant, le nombre de cibles à la surface des cellules est généralement limité, ce qui rend le TMDD saturable et entraîne une pharmacocinétique non linéaire.
- Métabolisme non spécifique : des processus non médiés par la cible, tels que la protéolyse et la pinocytose non spécifique, peuvent libérer des cytotoxines à petites molécules à des sites involontaires, provoquant des effets secondaires hors cible.
- Immunogénicité : les PDC peuvent déclencher l'immunogénicité, stimulant la production d'anticorps anti-médicament (ADA), qui neutralisent le médicament et forment des complexes éliminés par le système immunitaire. Il est important de noter que l’immunogénicité ou les réponses ADA observées chez les animaux précliniques ne prédisent pas les réponses ADA humaines.
ExcrétionLes PDC, dont le poids moléculaire est bien inférieur au seuil de filtration rénale (60 kDa), sont rapidement éliminés par les reins, empêchant ainsi une accumulation efficace de cytotoxines dans les tumeurs. Par conséquent, des modifications ou des altérations chimiques des peptides hôtes des PDC sont nécessaires pour améliorer la stabilité et prolonger la demi-vie. L'excrétion rénale peut être la principale voie d'élimination de certains peptides ou médicaments PDC. Dans de tels cas, il est crucial de considérer que le taux de clairance calculé à partir de l'analyse non compartimentale (ANC) après l'administration IV doit être référencé au débit de filtration glomérulaire du médicament plutôt qu'au débit sanguin hépatique.
Stratégies d'étude pharmacocinétique pour les PDC
Les PDC utilisent intrinsèquement des stratégies de ciblage pour l’administration de médicaments, combinant les caractéristiques des médicaments à grosses et petites molécules. En raison de leur relative instabilité et de leurs problèmes de ciblage, la toxicité potentielle de la charge utile nécessite une attention particulière. Dans la phase de sélection des médicaments, les études DMPK se concentrent sur l'amélioration de la stabilité des peptides et des PDC dans le sang total, le plasma et l'homogénat rénal, tout en continuant à optimiser la structure des PDC grâce à l'identification in vitro et in vivo des métabolites afin d'améliorer la stabilité et la demi-vie. Il est recommandé de mener des études de distribution tissulaire chez les rongeurs au début du projet afin d'évaluer la toxicité potentielle de la charge utile pour différents organes.
Au stade du candidat clinique, des modèles in vitro appropriés doivent être identifiés pour évaluer et valider la libération in vivo de la charge utile. Les expériences in vivo devraient mesurer simultanément la concentration sanguine de PDC et de charge utile. Dans des conditions de dosage répétées, il est conseillé de surveiller les effets de l'ADA. Mener des expériences de distribution tissulaire chez les espèces PD est nécessaire pour évaluer la capacité de ciblage des PDC.
Conclusion et perspectives
Malgré la vaste expérience dans le développement de médicaments ADC, le développement de médicaments PDC n’est pas un chemin simple mais rempli à la fois d’opportunités et de défis. Par rapport aux ADC, la spécificité tissulaire et le ciblage tumoral des peptides sont quelque peu inférieurs, ce qui pose des défis importants pour la sélection des peptides de ciblage. De plus, en raison de la faible stabilité des peptides, leur administration orale présente des difficultés considérables. Les PDC sont également confrontés à des défis analytiques et à des effets potentiellement hors cible.
La conception des médicaments PDC intègre les avantages du ciblage des peptides et de divers types de médicaments. Les récentes approbations réglementaires de médicaments thérapeutiques par radionucléides et d’agents de diagnostic mettent en évidence le potentiel de ces médicaments. Les résultats cliniques encourageants des pipelines cliniques en cours soulignent encore davantage leur promesse. Avec la conjugaison de diverses entités moléculaires et le ciblage de peptides, le développement de médicaments PDC présente un grand potentiel pour l’avenir.